Сущность этого метода заключается в том, что в качестве электролита используют водные растворы солей тех металлов, которые необходимо получить в покрытии. Наиболее широкое применение для восстановления деталей нашли такие способы гальванического покрытия, как железнение (иногда этот процесс называют осталиванием, что не совсем правильно), хромирование (реже — никелирование) и электролитическое натирание.
Рассмотрим этот метод восстановления деталей на конкретных примерах, поскольку вы уже ознакомились в курсе химии с особенностями гальванического осаждения металла.
Железнение состоит в получении твердых износостойких железных покрытий из горячих хлористых электролитов. Детали, предназначенные для покрытия, являются катодами, а анодами — растворимые электроды (обычно из стали 08 или 10). При растворении анода выделяются вещества, образующие шлам, поэтому во избежание загрязнения электролита электроды помещают в чехлы из стеклоткани.
Рассмотрим процесс железнения на примере восстановления поршневых пальцев ДВС (рис. 2.13). После мойки, тщательной очистки и обезжиривания поверхности, предназначенной для осаждения покрытия, деталь подвешивают на катод (отрицательный электрод), обеспечивая надежность контакта, например, с помощью цангового разжимного приспособления. При прохождении тока через электролит молекулы соли в воде подвергаются электролитической диссоциации на положительно заряженные ионы (катионы), которые перемешаются к детали (катоду), и отрицательно заряженные ионы (анионы), которые перемещаются к аноду.
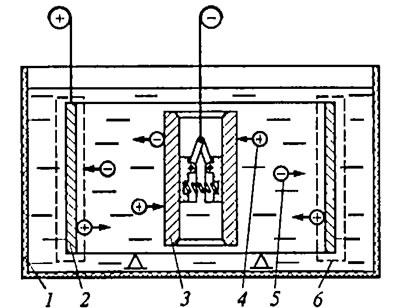
Рис. 2.13. Восстановление поршневых пальцев гальваническим осаждением покрытий: 1 - ванна (неметаллическая), 2 - электрод (свинец); 3 - деталь; 4 - катион; 5 - анион; 6 - сетка (неметаллическая)
В результате катион, коснувшись поверхности детали, получает недостающий электрон, превращается в нейтральный атом и осаждается на поверхности. При этом выделяется водород Н2. В свою очередь, анион, коснувшись анода, теряет свой заряд и превращается в нейтральный атом с выделением кислорода О2 и кислотного остатка.
Применяемый электролит имеет следующий химический состав, г/л:
- Водный раствор хлорида железа FeCl2·4H2O — 400±20
- Соляная кислота HCl — 2±0,2
- Хлорид марганца MnCl2·4Н2О — 10±2
Эффективность процесса осаждения характеризуется коэффициентом выхода металла по току а, показывающим какой процент тока вызывает отложение металла на катоде (табл. 2.3).
Масса вещества, выделяющегося при электролизе на катоде (согласно закону Фарадея).
Таблица 2.3. Значения величин α и с для основных металлов, используемых при восстановлении деталей гальваническим методом
| Параметр | Fe | Cr | Ni | Cu (из электролита) | Zn |
| α, % | 85...95 | 13... 18 | 90 | 98 | 92 |
| с, г/(А·ч) | 1,042 | 0,342 | 1,095 | 1,186 (кислого) 2,372 (цианистого) | 1,220 |
где с — электрохимический эквивалент металла, г/(А ч); I — сила тока, А; t — продолжительность электролиза, ч.
Толщина осажденного слоя h, мм, при условии равномерного осаждения его на заданном участке поверхности детали определяется соотношением
где Dк=I/F — катодная плотность тока, А/дм2; ρ — плотность осаждаемого металла, г/см3; F — площадь поверхности детали, дм2.
Равномерность толщины h в значительной степени зависит от рассеивающей способности электролита, связанной, например, с однородностью электрического поля.
Процесс железнения имеет ряд преимуществ перед хромированием:
- 1) высокий (в 5 —6 раз выше, чем при хромировании) выход металла по току, достигающий 85...90%;
- 2) большая (в 10—15 раз) скорость нанесения покрытия, которая достигает 0,3...0,5 мм/ч;
- 3) повышенная износостойкость покрытия (не ниже, чем у закаленной стали 45);
- 4) возможность получения высокопрочных покрытий толщиной более 1 мм;
- 5) применение более простого по составу и дешевого электролита;
- 6) повышенная прочность сцепления покрытия с подложкой (при осаждении на стальные детали предел прочности составляет 400...450 МПа).
На качество покрытия и его твердость непосредственное влияние оказывают плотность тока и температура электролита. Для повышения качества покрытия и интенсификации процесса железнения рекомендуется применять нестационарные электрические режимы с применением переменного тока. Использование проточного электролита снижает поляризацию электродов и способствует их очистке, что в итоге обеспечивает повышение производительности в 10—15 раз и получение беспористого высокопрочного покрытия.
Хромирование применяется для восстановления деталей при незначительном износе рабочей поверхности детали, а именно, до 0,1 мм Учитывая высокую твердость наносимого слоя, хромирование осуществляют в основном с целью повышения износостойкости трущихся пар. В качестве электролита используют водный раствор хромового ангидрида (CrO3) и серной кислоты (H2SO4).
